Таблица менделеева что все означает. Периодическая система химических элементов Д.И.Менделеева
В природе существует очень много повторяющихся последовательностей:
- времена года;
- время суток;
- дни недели…
В середине 19 века Д.И.Менделеев заметил, что химические свойства элементов также имеют определенную последовательность (говорят, что эта идея пришла ему во сне). Итогом чудесных сновидений ученого стала Периодическая таблица химических элементов, в которой Д.И. Менделеев выстроил химические элементы по возрастанию атомной массы. В современной таблице химические элементы выстроены по возрастанию атомного номера элемента (количество протонов в ядре атома).
Атомный номер изображен над символом химического элемента, под символом - его атомная масса (сумма протонов и нейтронов). Обратите внимание, что атомная масса у некоторых элементов является нецелым числом! Помните об изотопах! Атомная масса - это средневзвешенное от всех изотопов элемента, встречающихся в природе в естественных условиях.

Под таблицей расположены лантаноиды и актиноиды.
Металлы, неметаллы, металлоиды

Расположены в Периодической таблице слева от ступенчатой диагональной линии, которая начинается с Бора (В) и заканчивается полонием (Po) (исключение составляют германий (Ge) и сурьма (Sb). Нетрудно заметить, что металлы занимают бОльшую часть Периодической таблицы. Основные свойства металлов: твердые (кроме ртути); блестят; хорошие электро- и теплопроводники; пластичные; ковкие; легко отдают электроны.

Элементы, расположенные справа от ступенчатой диагонали B-Po, называются неметаллами . Свойства неметаллов прямо противоположны свойствам металлов: плохие проводники тепла и электричества; хрупкие; нековкие; непластичные; обычно принимают электроны.
Металлоиды
Между металлами и неметаллами находятся полуметаллы (металлоиды). Для них характерны свойства как металлов, так и неметаллов. Основное применение в промышленности полуметаллы нашли в производстве полупроводников, без которых немыслима ни одна современная микросхема или микропроцессор.
Периоды и группы
Как уже говорилось выше, периодическая таблица состоит из семи периодов. В каждом периоде атомные номера элементов увеличиваются слева направо.
Свойства элементов в периодах изменяются последовательно: так натрий (Na) и магний (Mg), находящиеся в начале третьего периода, отдают электроны (Na отдает один электрон: 1s 2 2s 2 2p 6 3s 1 ; Mg отдает два электрона: 1s 2 2s 2 2p 6 3s 2). А вот хлор (Cl), расположенный в конце периода, принимает один элемент: 1s 2 2s 2 2p 6 3s 2 3p 5 .
В группах же, наоборот, все элементы обладают одинаковыми свойствами. Например, в группе IA(1) все элементы, начиная с лития (Li) и заканчивая францием (Fr), отдают один электрон. А все элементы группы VIIA(17), принимают один элемент.
Некоторые группы настолько важны, что получили особые названия. Эти группы рассмотрены ниже.
Группа IA(1) . Атомы элементов этой группы имеют во внешнем электронном слое всего по одному электрону, поэтому легко отдают один электрон.
Наиболее важные щелочные металлы - натрий (Na) и калий (K), поскольку играют важную роль в процессе жизнедеятельности человека и входят в состав солей.
Электронные конфигурации:
- Li - 1s 2 2s 1 ;
- Na - 1s 2 2s 2 2p 6 3s 1 ;
- K - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
Группа IIA(2) . Атомы элементов этой группы имеют во внешнем электронном слое по два электрона, которые также отдают во время химических реакций. Наиболее важный элемент - кальций (Ca) - основа костей и зубов.
Электронные конфигурации:
- Be - 1s 2 2s 2 ;
- Mg - 1s 2 2s 2 2p 6 3s 2 ;
- Ca - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2
Группа VIIA(17) . Атомы элементов этой группы обычно получают по одному электрону, т.к. на внешнем электронном слое находится по пять элементов и до "полного комплекта" как раз не хватает одного электрона.
Наиболее известные элементы этой группы: хлор (Cl) - входит в состав соли и хлорной извести; йод (I) - элемент, играющий важную роль в деятельности щитовидной железы человека.
Электронная конфигурация:
- F - 1s 2 2s 2 2p 5 ;
- Cl - 1s 2 2s 2 2p 6 3s 2 3p 5 ;
- Br - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5
Группа VIII(18). Атомы элементов этой группы имеют полностью "укомплектованный" внешний электронный слой. Поэтому им "не надо" принимать электроны. И отдавать их они "не хотят". Отсюда - элементы этой группы очень "неохотно" вступают в химические реакции. Долгое время считалось, что они вообще не вступают в реакции (отсюда и название "инертный", т.е. "бездействующий"). Но химик Нейл Барлетт открыл, что некоторые из этих газов при определенных условиях все же могут вступать в реакции с другими элементами.
Электронные конфигурации:
- Ne - 1s 2 2s 2 2p 6 ;
- Ar - 1s 2 2s 2 2p 6 3s 2 3p 6 ;
- Kr - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6
Валентные элементы в группах
Нетрудно заметить, что внутри каждой группы элементы похожи друг на друга своими валентными электронами (электроны s и p-орбиталей, расположенных на внешнем энергетическом уровне).
У щелочных металлов - по 1 валентному электрону:
- Li - 1s 2 2s 1 ;
- Na - 1s 2 2s 2 2p 6 3s 1 ;
- K - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
У щелочноземельных металлов - по 2 валентных электрона:
- Be - 1s 2 2s 2 ;
- Mg - 1s 2 2s 2 2p 6 3s 2 ;
- Ca - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2
У галогенов - по 7 валентных электронов:
- F - 1s 2 2s 2 2p 5 ;
- Cl - 1s 2 2s 2 2p 6 3s 2 3p 5 ;
- Br - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5
У инертных газов - по 8 валентных электронов:
- Ne - 1s 2 2s 2 2p 6 ;
- Ar - 1s 2 2s 2 2p 6 3s 2 3p 6 ;
- Kr - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6
Дополнительную информацию см. в статье Валентность и в Таблице электронных конфигураций атомов химических элементов по периодам .
Обратим теперь свое внимание на элементы, расположенные в группах с символов В . Они расположены в центре периодической таблицы и называются переходными металлами .
Отличительной особенностью этих элементов является присутствие в атомах электронов, заполняющих d-орбитали :
- Sc - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 ;
- Ti - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2
Отдельно от основной таблицы расположены лантаноиды и актиноиды - это, так называемые, внутренние переходные металлы . В атомах этих элементов электроны заполняют f-орбитали :
- Ce - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 4d 10 5s 2 5p 6 4f 1 5d 1 6s 2 ;
- Th - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 4d 10 5s 2 5p 6 4f 14 5d 10 6s 2 6p 6 6d 2 7s 2
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Построение периодической таблицы химических элементов Менделеева отвечает характерным периодам теории чисел и ортогональных базисов. Дополнение матриц Адамара матрицами четных и нечетных порядков создает структурный базис вложенных матричных элементов: матриц первого (Odin), второго (Euler), третьего (Mersenne), четвертого (Hadamard) и пятого (Fermat) порядков.
Несложно заметить, что порядкам 4k матриц Адамара соответствуют инертные элементы с атомной массой, кратной четырем: гелий 4, неон 20, аргон 40 (39.948) и т.п., но также и основы жизни и цифровой техники: углерод 12, кислород 16, кремний 28, германий 72.
Такое впечатление, что с матрицами Мерсенна порядков 4k –1, напротив, связано все активное, ядовитое, разрушительное и разъедающее. Но это также радиоактивные элементы – источники энергии, и свинец 207 (конечный продукт, ядовитые соли). Фтор, это, конечно, 19. Порядкам матриц Мерсенна отвечает последовательность радиоактивных элементов, называемая рядом актиния: уран 235, плутоний 239 (изотоп, который является более мощным источником атомной энергии, чем уран) и т.п. Это также щелочные металлы литий 7, натрий 23 и калий 39.

Галлий – атомный вес 68
Порядкам 4k –2 матриц Эйлера (сдвоенный Мерсенн) соответствует азот 14 (основа атмосферы). Поваренная соль образована двумя "мерсенноподобными" атомами натрия 23 и хлора 35, вместе это сочетание характерно, как раз, для матриц Эйлера. Более массивный хлор с весом 35.4 немногим не добирает до адамаровой размерности 36. Кристаллы поваренной соли: куб (! т.е. характер смирный, адамаров) и октаэдр (более вызывающий, это несомненный Эйлер).
В атомной физике переход железо 56 – никель 59, это рубеж между элементами, дающими энергию при синтезе более крупного ядра (водородная бомба) и распаде (урановая). Порядок 58 знаменит тем, что для него нет не только аналогов матриц Адамара в виде матриц Белевича с нулями на диагонали, для него нет и многих взвешенных матриц – ближайшая ортогональная W(58,53) имеет 5 нулей в каждом столбце и строке (глубокий разрыв).
В ряду, соответствующем матрицам Ферма и их замещениям порядков 4k +1, стоит волею судьбы фермий 257. Ничего не скажешь, точное попадание. Здесь же золото 197. Медь 64 (63.547) и серебро 108 (107.868), символы электроники, недотягивают, как видно, до золота и соответствуют более скромным матрицам Адамара. Медь, с ее недалеко ушедшим от 63 атомным весом, химически активна – ее зеленые окислы хорошо известны.

Кристаллы бора под сильным увеличением
С золотым сечением связан бор – атомная масса среди всех прочих элементов наиболее близка к 10 (точнее 10.8, близость атомного веса к нечетным числам тоже сказывается). Бор – достаточно сложный элемент. Бор играет запутанную роль в истории самой жизни. Строение каркаса в его структурах гораздо сложнее, чем в алмазе. Уникальный тип химической связи, которая позволяет бору поглощать любую примесь, очень плохо изучен, хотя за исследования, связанные с ним, большое количество ученых уже получили Нобелевские премии. Форма кристалла бора – икосаэдр, пять треугольников образуют вершину.
Загадка Платины. Пятый элемент, это, без сомнения, благородные металлы, такие, как золото. Надстройка над адамаровой размерностью 4k , на 1 большие.

Стабильный изотоп уран 238
Вспомним, все же, что числа Ферма встречаются редко (ближайшее – 257). Кристаллы самородного золота имеют форму, близкую к кубу, но и пентаграмма просверкивает. Его ближайший сосед, платина, благородный металл, отстоит от золота 197 по атомному весу меньше, чем на 4. Платина имеет атомный вес не 193, а несколько повышенный, 194 (порядок матриц Эйлера). Мелочь, но это переносит ее в стан несколько более агрессивных элементов. Стоит вспомнить, в связи, что при ее инертности (растворяется, разве, в царской водке), платину используют как активный катализатор химических процессов.
Губчатая платина при комнатной температуре воспламеняет водород. Характер у платины вовсе не мирный, смирнее себя ведет иридий 192 (смесь изотопов 191 и 193). Это, скорее, медь, но с весом и характером золота.
Между неоном 20 и натрием 23 нет элемента с атомным весом 22. Конечно, атомные веса – интегральная характеристика. Но среди изотопов, в свою очередь, тоже наблюдается любопытная корреляция свойств со свойствами чисел и соответствующих им матриц ортогональных базисов. В качестве ядерного топлива наибольшее применение имеет изотоп уран 235 (порядок матриц Мерсенна), в котором возможна самоподдерживающаяся цепная ядерная реакция. В природе этот элемент распространен стабильной форме уран 238 (порядок матриц Эйлера). Элемент с атомным весом 13 отсутствует. Что касается хаоса, то ограниченное количество устойчивых элементов таблицы Менделеева и сложность нахождения уровневых матриц высоких порядков ввиду замеченного у матриц тринадцатого порядка барьера коррелируют.
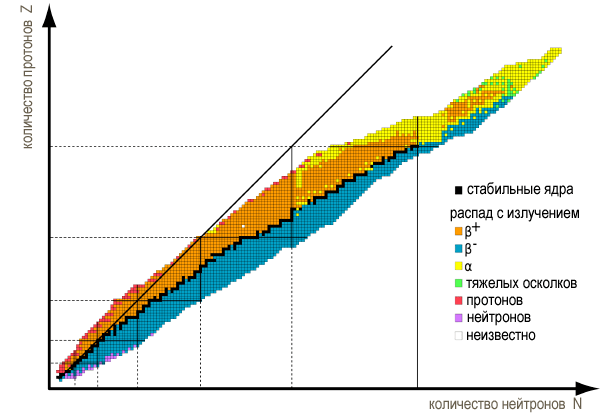
Изотопы химических элементов, островок стабильности
115 элемент таблицы Менделеева - московий (moscovium) - сверхтяжелый синтетический элемент с символом Mc и атомным номером 115. Он был впервые получен в 2003 году совместной командой российских и американских ученых в Объединенном институте ядерных исследований (ОИЯИ) в Дубне, Россия. В декабре 2015 года признан одним из четырех новых элементов Объединенной рабочей группой международных научных организаций IUPAC/IUPAP. 28 ноября 2016 года он был официально назван в честь Московского региона, в котором находится ОИЯИ.
Характеристика
115 элемент таблицы Менделеева является чрезвычайно радиоактивным веществом: его наиболее стабильный известный изотоп, moscovium-290 имеет период полураспада всего 0,8 секунды. Ученые относят московий к непереходным металлам, по ряду характеристик схожим с висмутом. В периодической таблице относится к трансактинидным элементам p-блока 7-го периода и помещен в группу 15 как самый тяжелый пниктоген (элемент подгруппы азота), хотя и не подтверждено, что он ведет себя, как более тяжелый гомолог висмута.
Согласно расчетам, элемент обладает некоторыми свойствами, схожими с более легкими гомологами: азотом, фосфором, мышьяком, сурьмой и висмутом. При этом демонстрирует несколько существенных отличий от них. На сегодня синтезировано около 100 атомов московия, которые имеют массовые числа от 287 до 290.

Физические свойства
Валентные электроны 115 элемента таблицы Менделеева московия делятся на три подоболочки: 7s (два электрона), 7p 1/2 (два электрона) и 7p 3/2 (один электрон). Первые два из них релятивистски стабилизируются и, следовательно, ведут себя, как инертные газы, а последние релятивистски дестабилизируются и могут легко участвовать в химических взаимодействиях. Таким образом, первичный потенциал ионизации московия должен составлять около 5,58 эВ. Согласно расчетам, moscovium должен быть плотным металлом из-за его высокого атомного веса с плотностью около 13,5 г/см 3 .
Предполагаемые расчетные характеристики:
- Фаза: твердая.
- Температура плавления: 400°С (670°К, 750°F).
- Точка кипения: 1100°С (1400°К, 2000°F).
- Удельная теплота плавления: 5,90-5,98 кДж/моль.
- Удельная теплота парообразования и конденсации: 138 кДж/моль.

Химические свойства
115-й элемент таблицы Менделеева стоит третьим в ряду химических элементов 7p и является самым тяжелым членом группы 15 в периодической таблице, располагаясь ниже висмута. Химическое взаимодействие московия в водном растворе обусловлено характеристиками ионов Mc + и Mc 3+ . Первые, предположительно, легко гидролизуются и образуют ионную связь с галогенами, цианидами и аммиаком. Гидроксид московия (I) (McOH), карбонат (Mc 2 CO 3), оксалат (Mc 2 C 2 O 4) и фторид (McF) должны растворяться в воде. Сульфид (Мс 2 S) должен быть нерастворимым. Хлорид (McCl), бромид (McBr), йодид (McI) и тиоцианат (McSCN) - слаборастворимые соединения.
Фторид московия (III) (McF 3) и тиозонид (McS 3), предположительно, нерастворимы в воде (аналогично соответствующим соединениям висмута). В то время, как хлорид (III) (McCl 3), бромид (McBr 3) и иодид (McI 3) должны быть легко растворимы и легко гидролизованы с образованием оксогалогенидов, таких как McOCl и McOBr (также аналогично висмуту). Оксиды московия (I) и (III) обладают схожими состояниями окисления, и их относительная стабильность в значительной степени зависит от того, с какими элементами они взаимодействуют.
Неопределенность
Вследствие того, что 115 элемент таблицы Менделеева синтезируется единичными экспериментально его точные характеристики проблематично. Ученым приходится ориентироваться на теоретические расчеты и сравнивать с более стабильными элементами, схожими по свойствам.
В 2011 году были проведены эксперименты по созданию изотопов нихония, флеровия и московия в реакциях между «ускорителями» (кальцием-48) и «мишенями» (америцием-243 и плутонием-244) для исследования их свойств. Однако «мишени» включали примеси свинца и висмута и, следовательно, были получены в реакциях переноса нуклонов некоторые изотопы висмута и полония, что осложнило проведение эксперимента. Между тем, полученные данные помогут в будущем ученым более детально исследовать тяжелые гомологи висмута и полония, такие как moscovium и livermorium.

Открытие
Первым успешным синтезом 115 элемента таблицы Менделеева была совместная работа российских и американских ученых в августе 2003 года в ОИЯИ в Дубне. В команду во главе с физиком-ядерщиком Юрием Оганесяном, помимо отечественных специалистов, вошли коллеги из Ливерморской национальной лаборатории Лоуренса. Исследователи 2 февраля 2004 года опубликовали в издании Physical Review информацию, что они бомбардировали америций-243 ионами кальция-48 на циклотроне У-400 и получили четыре атома нового вещества (одно ядро 287 Mc и три ядра 288 Mc). Эти атомы затухают (распадаются) за счет эмиссии альфа-частиц до элемента нихония примерно за 100 миллисекунд. Два более тяжелых изотопа московия, 289 Mc и 290 Mc, были обнаружены в 2009-2010 годах.
Первоначально IUPAC не могла утвердить открытие нового элемента. Требовалось подтверждение из других источников. В течение следующих нескольких лет была проведена еще одна оценка более поздних экспериментов, и еще раз выдвинуто заявление дубненской команды об открытии 115-го элемента.
В августе 2013 года группа исследователей из Университета Лунда и Института тяжелых ионов в Дармштадте (Германия) объявили, что они повторили эксперимент 2004 года, подтвердив результаты, полученные в Дубне. Еще одно подтверждение было опубликовано командой ученых, работавших в Беркли в 2015 году. В декабре 2015 года совместная рабочая группа IUPAC/IUPAP признала обнаружение этого элемента и отдала приоритет в открытии российско-американской команде исследователей.

Название
115 элемент таблицы Менделеева в 1979 году согласно рекомендации IUPAC было решено назвать «унунпентий» и обозначать соответствующим символом UUP. Несмотря на то, что данное название с тех пор широко использовалось в отношении неоткрытого (но теоретически предсказанного) элемента, в сообществе физиков оно не прижилось. Чаще всего вещество так и называли - элемент №115 или E115.
30 декабря 2015 года обнаружение нового элемента было признано Международным союзом чистой и прикладной химии. Согласно новым правилам, первооткрыватели имеют право предложить собственное название нового вещества. Сначала предполагалось назвать 115 элемент таблицы Менделеева «лангевиний» в честь физика Поля Ланжевена. Позднее команда ученых из Дубны, как вариант, предложила наименование «московий» в честь Московской области, где и было совершено открытие. В июне 2016 года IUPAC одобрил инициативу и 28 ноября 2016 официально утвердил название «moscovium».
Очень много различных вещей и предметов, живых и неживых тел природы нас окружает. И все они имеют свой состав, строение, свойства. В живых существах протекают сложнейшие биохимические реакции, сопровождающие процессы жизнедеятельности. Неживые тела выполняют различные функции в природе и жизни биомассы и имеют сложный молекулярный и атомарный состав.
Но все вместе объекты планеты имеют общую особенность: они состоят из множества мельчайших структурных частиц, называемых атомами химических элементов. Настолько мелких, что невооруженным взглядом их не рассмотреть. Что такое химические элементы? Какими характеристиками они обладают и откуда стало известно об их существовании? Попробуем разобраться.
Понятие о химических элементах
В общепринятом понимании химические элементы - это лишь графическое отображение атомов. Частиц, из которых складывается все существующее во Вселенной. То есть на вопрос "что такое химические элементы" можно дать такой ответ. Это сложные маленькие структуры, совокупности всех изотопов атомов, объединенные общим названием, имеющие свое графическое обозначение (символ).
На сегодняшний день известно о 118 элементах, которые открыты как в естественных условиях, так и синтетически, путем осуществления ядерных реакций и ядер других атомов. Каждый из них имеет набор характеристик, свое местоположение в общей системе, историю открытия и название, а также выполняет определенную роль в природе и жизни живых существ. Изучением этих особенностей занимается наука химия. Химические элементы - это основа для построения молекул, простых и сложных соединений, а следовательно, химических взаимодействий.
История открытия
Само понимание того, что такое химические элементы, пришло только в XVII веке благодаря работам Бойля. Именно он впервые заговорил об этом понятии и дал ему следующее определение. Это неделимые маленькие простые вещества, из которых складывается все вокруг, в том числе и все сложные.
До этой работы господствовали взгляды алхимиков, признававшим теорию четырех стихий - Эмпидокла и Аристотеля, а также открывших "горючие начала" (сера) и "металлические начала" (ртуть).
Практически весь XVIII век была распространена совершенно ошибочная теория флогистона. Однако уже в конце этого периода Антуан Лоран Лавуазье доказывает, что она несостоятельна. Он повторяет формулировку Бойля, но при этом дополняет ее первой попыткой систематизации всех известных на тот момент элементов, распределив их на четыре группы: металлы, радикалы, земли, неметаллы.

Следующий большой шаг в понимании того, что такое химические элементы, делает Дальтон. Ему принадлежит заслуга открытия атомной массы. На основе этого он распределяет часть известных химических элементов в порядке возрастания их атомной массы.
Стабильно интенсивное развитие науки и техники позволяет делать ряд открытий новых элементов в составе природных тел. Поэтому к 1869 году - времени великого творения Д. И. Менделеева - науке стало известно о существовании 63 элементов. Работа русского ученого стала первой полной и навсегда закрепившейся классификацией этих частиц.
Строение химических элементов на тот момент установлено не было. Считалось, что атом неделим, что это мельчайшая единица. С открытием явления радиоактивности было доказано, что он делится на структурные части. Практически каждый при этом существует в форме нескольких природных изотопов (аналогичных частиц, но с иным количеством структур нейтронов, от чего меняется атомная масса). Таким образом, к середине прошлого столетия удалось добиться порядка в определении понятия химического элемента.
Система химических элементов Менделеева
В основу ученый положил различие в атомной массе и сумел гениальным образом расположить все известные химические элементы в порядке ее возрастания. Однако вся глубина и гениальность его научного мышления и предвидения заключалась в том, что Менделеев оставил пустые места в своей системе, открытые ячейки для еще неизвестных элементов, которые, по мнению ученого, в будущем будут открыты.
И все получилось именно так, как он сказал. Химические элементы Менделеева с течением времени заполнили все пустые ячейки. Была открыта каждая предсказанная ученым структура. И теперь мы можем смело говорить о том, что система химических элементов представлена 118 единицами. Правда, три последних открытия пока еще официально не подтверждены.
Сама по себе система химических элементов отображается графически таблицей, в которой элементы располагаются согласно иерархичности их свойств, зарядам ядер и особенностям строения электронных оболочек их атомов. Так, имеются периоды (7 штук) - горизонтальные ряды, группы (8 штук) - вертикальные, подгруппы (главная и побочная в пределах каждой группы). Чаще всего отдельно в нижние слои таблицы выносятся два ряда семейств - лантаноиды и актиноиды.

Атомная масса элемента складывается из протонов и нейтронов, совокупность которым имеет название "массовое число". Количество протонов определяется очень просто - оно равно порядковому номеру элемента в системе. А так как атом в целом - система электронейтральная, то есть не имеющая вообще никакого заряда, то количество отрицательных электронов всегда равно количеству положительных частиц протонов.
Таким образом, характеристика химического элемента может быть дана по его положению в периодической системе. Ведь в ячейке описано практически все: порядковый номер, а значит, электроны и протоны, атомная масса (усредненное значение всех существующих изотопов данного элемента). Видно, в каком периоде находится структура (значит, на стольких слоях будут располагаться электроны). Также можно предсказать количество отрицательных частиц на последнем энергетическом уровне для элементов главных подгрупп - оно равно номеру группы, в которой располагается элемент.

Количество нейтронов можно рассчитать, если вычесть из массового числа протоны, то есть порядковый номер. Таким образом, можно получить и составить целую электронно-графическую формулу для каждого химического элемента, которая будет в точности отражать его строение и показывать возможные и проявляемые свойства.
Распространение элементов в природе
Изучением этого вопроса занимается целая наука - космохимия. Данные показывают, что распределение элементов по нашей планете повторяет такие же закономерности во Вселенной. Главным источником ядер легких, тяжелых и средних атомов являются ядерные реакции, происходящие в недрах звезд - нуклеосинтез. Благодаря этим процессам Вселенная и космическое пространство снабдили нашу планету всеми имеющимися химическими элементами.
Всего из известных 118 представителей в естественных природных источниках людьми были обнаружены 89. Это основополагающие, самые распространенные атомы. Химические элементы также были синтезированы искусственно, путем бомбардировки ядер нейтронами (нуклеосинтез в лабораторных условиях).

Самыми многочисленными считаются простые вещества таких элементов, как азот, кислород, водород. Углерод входит в состав всех органических веществ, а значит, также занимает лидирующие позиции.
Классификация по электронному строению атомов
Одна из самых распространенных классификаций всех химических элементов системы - это распределение их на основе электронного строения. По тому, сколько энергетических уровней входит в состав оболочки атома и который из них содержит последние валентные электроны, можно выделить четыре группы элементов.
S-элементы
Это такие, у которых последней заполняется s-орбиталь. К этому семейству относятся элементы первой группы главной подгруппы (или Всего один электрон на внешнем уровне определяет схожие свойства этих представителей как сильных восстановителей.
Р-элементы
Всего 30 штук. Валентные электроны располагаются на р-подуровне. Это элементы, формирующие главные подгруппы с третьей по восьмую группу, относящиеся к 3,4,5,6 периодам. Среди них по свойствам встречаются как металлы, так и типичные неметаллические элементы.
d-элементы и f-элементы
Это переходные металлы с 4 по 7 большой период. Всего 32 элемента. Простые вещества могут проявлять как кислотные, так и основные свойства (окислительные и восстановительные). Также амфотерные, то есть двойственные.
К f-семейству относятся лантаноиды и актиноиды, у которых последние электроны располагаются на f-орбиталях.
Вещества, образуемые элементами: простые
Также все классы химических элементов способны существовать в виде простых или сложных соединений. Так, простыми принято считать такие, которые образованы из одной и той же структуры в разном количестве. Например, О 2 - кислород или дикислород, а О 3 - озон. Такое явление носит название аллотропии.

Простые химические элементы, формирующие одноименные соединения, характерны для каждого представителя периодической системы. Но не все они одинаковы по проявляемым свойствам. Так, существуют простые вещества металлы и неметаллы. Первые образуют главные подгруппы с 1-3 группу и все побочные подгруппы в таблице. Неметаллы же формируют главные подгруппы 4-7 групп. В восьмую основную входят особые элементы - благородные или инертные газы.
Среди всех открытых на сегодня простых элементов известны при обычных условиях 11 газов, 2 жидких вещества (бром и ртуть), все остальные - твердые.
Сложные соединения
К таковым принято относить все, которые состоят из двух и более химических элементов. Примеров масса, ведь химических соединений известно более 2 миллионов! Это соли, оксиды, основания и кислоты, сложные комплексные соединения, все органические вещества.
Эфир в таблице Менделеева
Мировой эфир есть субстанция ВСЯКОГО химического элемента и значит - ВСЯКОГО вещества, есть Абсолютная истинная материя как Всемирная элементообразующая Сущность. Мировой эфир - это исток и венец всей подлинной Таблицы Менделеева, её начало и конец, - альфа и омега Периодической системы элементов Дмитрия Ивановича Менделеева.
В античной философии эфир (aithér-греч) наряду с землей, водой, воздухом и огнем - один из пяти элементов бытия (по Аристотелю) - пятая сущность (quinta essentia -лат.), понимаемая как тончайшая всепроникающая материя. В конце XIX века в ученых кругах получила широкое хождение гипотеза о мировом эфире (МЭ), заполняющем все мировое пространство. Он понимался как невесомая и упругая жидкость, которая пронизывает все тела. Существованием эфира пытались объяснить многие физические явления и свойства.
Предисловие.
У Менделеева было два фундаментальных научных открытия:
1 - Открытие Периодического закона в субстанции химии,
2 - Открытие взаимосвязи субстанции химии и субстанции Эфира, а именно: частицы Эфира формирует молекулы, ядра, электроны и т.д., но в химических реакциях не участвуют.
Эфир - частицы вещества размером ~ 10-100 метра (фактически - «первокирпичики» материи).
Факты. В подлинной таблице Менделеева был Эфир. Ячейка для Эфира располагалась в нулевой группе с инертными газами и в нулевом ряду как главный системообразующий фактор для построения Системы химических элементов. После смерти Менделеева таблицу исказили, убрав из неё Эфир и отменив нулевую группу, тем самым, скрыв фундаментальное открытие концептуального значения.
В современных таблицах Эфира: 1 - не видно, 2 - и не угадывается (из-за отсутствия нулевой группы).
Такой целенаправленный подлог сдерживает развитие прогресса цивилизации.
Техногенные катастрофы (напр. Чернобыль и Фукусима) были бы исключены, если бы в развитие подлинной таблицы Менделеева своевременно были вложены адекватные ресурсы. Сокрытие концептуальных знаний идёт на глобальном уровне для «опускания» цивилизации.
Результат. В школах и ВУЗах преподают обрезанную таблицу Менделеева.
Оценка ситуации. Таблица Менделеева без Эфира - то же самое, что человечество без детей - прожить можно, но развития и будущего не будет.
Резюме. Если враги человечества знания скрывают, то наша задача - эти знания раскрывать.
Вывод. В старой таблице Менделеева элементов меньше, а форсайта больше, чем в современной.
Заключение. Новый уровень возможен только при изменении информационного состояния общества.
Итог. Возврат к истинной таблице Менделеева - это уже вопрос не научный, а вопрос политический.

В чем же был основной политический смысл эйнштейновского учения? Он состоял в том, чтобы любыми путями перекрыть человечеству доступ к неисчерпаемым естественным источникам энергии, которые открывало изучение свойств мирового эфира . В случае успеха на этом пути, мировая финансовая олигархия теряла власть в этом мире, особенно в свете ретроспективы тех лет: Рокфеллеры сделали немыслимое состояние, превосходящее бюджет Соединенных Штатов, на нефтяных спекуляциях, и утрата той роли нефти, которую заняло «черное золото» в этом мире - роль крови мировой экономики - их не вдохновляла.
Не вдохновляло это и прочих олигархов - угольных и стальных королей. Так финансовый магнат Морган моментально прекратил финансирование экспериментов Николы Теслы, когда тот вплотную подошел к беспроводной передаче энергии и извлечению энергии «из ниоткуда» - из мирового эфира. После этого обладателю огромного количества воплощенных в практику технических решений не оказывал финансовой помощи никто - солидарность у финансовых воротил как у воров в законе и феноменальный нюх на то, откуда исходит опасность. Вот поэтому против человечества и была произведена диверсия под названием «Специальная Теория Относительности».
Один из первых ударов пришелся на таблицу Дмитрия Менделеева, в которой эфир стоял первым номером, именно размышления об эфире породили гениальное прозрение Менделеева - его периодическую таблицу элементов.

Глава из статьи: В.Г. Родионов. Место и роль мирового эфира в истинной таблице Д.И. Менделеева
6. Argumentum ad rem
То, что сейчас преподносят в школах и университетах под названием «Периодическая система химических элементов Д.И. Менделеева»,- откровенная ф а л ь ш и в к а.
Последний раз в неискажённом виде настоящая Таблица Менделеева увидела свет в 1906 году в Санкт-Петербурге (учебник «Основы химии», VIII издание). И только спустя 96 лет забвения подлинная Таблица Менделеева впервые восстаёт из пепла благодаря публикации диссертации в журнале ЖРФМ Русского Физического Общества.
После скоропостижной смерти Д. И. Менделеева и ухода из жизни его верных научных коллег по Русскому Физико-Химическому Обществу, впервые поднял руку на бессмертное творение Менделеева — сын друга и соратника Д. И. Менделеева по Обществу — Борис Николаевич Меншуткин. Конечно, Меншуткин действовал не в одиночку, — он лишь выполнял заказ. Ведь, новая парадигма релятивизма требовала отказа от идеи мирового эфира; и потому это требование было возведено в ранг догмы, а труд Д. И. Менделеева был фальсифицирован.
Главное искажение Таблицы — перенос «нулевой группы» Таблицы в её конец, вправо, и введение т.н. «периодов». Подчёркиваем, что такая (лишь на первый взгляд — безобидная) манипуляция логически объяснима только как сознательное устранение главного методологического звена в открытии Менделеева: периодическая система элементов в своём начале, истоке, т.е. в верхнем левом углу Таблицы, должна иметь нулевую группу и нулевой ряд, где располагается элемент «Х» (по Менделееву — «Ньютоний»),- т.е. мировой эфир.
Более того, являясь единственным системообразующим элементом всей Таблицы производных элементов, этот элемент «Х» есть аргумент всей Таблицы Менделеева. Перенос же нулевой группы Таблицы в её конец уничтожает саму идею этой первоосновы всей системы элементов по Менделееву.
Для подтверждения вышесказанного, предоставим слово самому Д. И. Менделееву.
«… Если же аналоги аргона вовсе не дают соединений, то очевидно, что нельзя включать ни одну из групп ранее известных элементов, и для них должно открыть особую группу нулевую … Это положение аргоновых аналогов в нулевой группе составляет строго логическое следствие понимания периодического закона, а потому (помещение в группе VIII явно не верно) принято не только мною, но и Браизнером, Пиччини и другими … Теперь же, когда стало не подлежать ни малейшему сомнению, что перед той I группой, в которой должно помещать водород, существует нулевая группа, представители которой имеют веса атомов меньше, чем у элементов I группы, мне кажется невозможным отрицать существование элементов более лёгких, чем водород.


Из них обратим внимание сперва на элемент первого ряда 1-й группы. Его означим через «y». Ему, очевидно, будут принадлежать коренные свойства аргоновых газов … «Короний», плотностью порядка 0,2 по отношению к водороду; и он не может быть ни коим образом мировым эфиром.
Этот элемент «у», однако, необходим для того, чтобы умственно подобраться к тому наиглавнейшему, а потому и наиболее быстро движущемуся элементу «х», который, по моему разумению, можно считать эфиром. Мне бы хотелось предварительно назвать его «Ньютонием» — в честь бессмертного Ньютона … Задачу тяготения и задачи всей энергетики (!!! — В.Родионов) нельзя представить реально решёнными без реального понимания эфира, как мировой среды, передающей энергию на расстояния. Реального же понимания эфира нельзя достичь, игнорируя его химизм и не считая его элементарным веществом; элементарные же вещества ныне немыслимы без подчинения их периодической законности»
(«Попытка химического понимания мирового эфира». 1905 г., стр. 27).

«Эти элементы, по величине их атомных весов, заняли точное место между галлоидами и щелочными металлами, как показал Рамзай в 1900 году. Из этих элементов необходимо образовать особую нулевую группу, которую прежде всех в 1900 году признал Еррере в Бельгии. Считаю здесь полезным присовокупить, что прямо судя по неспособности к соединениям элементов нулевой группы, аналогов аргона должно поставить раньше элементов 1 группы и по духу периодической системы ждать для них меньшего атомного веса, чем для щелочных металлов.
Это так и оказалось. А если так, то это обстоятельство, с одной стороны, служит подтверждением правильности периодических начал, а с другой стороны, ясно показывает отношение аналогов аргона к другим, ранее известным, элементам. Вследствие этого можно разбираемые начала прилагать ещё шире, чем ранее, и ждать элементов нулевого ряда с атомными весами гораздо меньшими, чем у водорода.
Таким образом, можно показать, что в первом ряду первым перед водородом существует элемент нулевой группы с атомным весом 0,4 (быть может, это короний Ионга), а в ряду нулевом, в нулевой группе — предельный элемент с ничтожно малым атомным весом, не способным к химическим взаимодействиям и обладающий вследствие того чрезвычайно быстрым собственным частичным (газовым) движением.
Эти свойства, быть может, должно приписать атомам всепроникающего (!!! — В.Родионов) мирового эфира. Мысль об этом указана мною в предисловии к этому изданию и в русской журнальной статье 1902 года …» («Основы химии». VIII изд., 1906 г., стр. 613 и след.)
1 , , ,
Из комментариев:
Для химии современной периодической таблицы элементов достаточно.
Роль эфира может быть полезна в ядерных реакциях, но и это слишком не значительно.
Учёт влияния эфира наиболее близко в явлениях распада изотопов. Однако учёт этот чрезвычайно сложен и наличие закономерностей принимаются не всеми учёными.
Самое простое доказательство наличия эфира: Явление аннигиляции позитрон-электронной пары и возникновение этой пары из вакуума, а также невозможность поймать электрон в состоянии покоя. Так же электромагнитное поле и полная аналогия между фотонами в вакууме и звуковыми волнами - фононами в кристаллах.
Эфир - это дифференцированная материя, так сказать, атомы в разобранном состоянии или правильней сказать, элементарные частицы, из которых формируются будущие атомы. Поэтому ему нет места в таблице Менделеева, так как логика построения данной системы не предполагает включать в её состав не целостные структуры,которыми являются сами атомы. В противном случае, так можно и для кварков найти место, где-нибудь в минус первом периоде.
Сам эфир имеет более сложную многоуровневую структуру проявления в мировом бытии, нежели об этом знает современная наука. Как только она раскроет первые тайны этого неуловимого эфира, тогда и будут изобретены новые двигатели для всевозможных машин на абсолютно новых принципах.
Действительно,Тесла едва ли не единственный, кто был близок к разгадке тайны, так называемого эфира,но ему сознательно мешали осуществить свои замыслы. Вот так до сегодняшнего дня ещё не родился тот гений, который продолжит дело великого изобретателя и расскажет всем нам, что же на самом деле представляет из себя таинственный эфир и на какой пьедестал его можно будет поставить.




